บทที่1 ความปลอดภัยและทักษะในการปฏิบัติการเคมี
1.1 ความปลอดภัยในการทำงานกับสารเคมี
การทำปฎิบัติการเคมีส่วนใหญ่ต้องมีความเกี่ยวข้องกับสารเคมี อุปกรณ์และเครื่องมือต่างๆซึ่งผู้ทำปฎิบัติการต้องตระหนักถึงความปลอดภัยของตนเอง ผู้อื่น และสิ่งแวดล้อม
1.1.1 ประเภทของสารเคมี
สารเคมีมีหลายประเภท แต่ละประเภทมีสมบัติแตกต่างกัน สารเคมีจึงจำเป็นต้องมีฉลากที่มีข้อมูลเกี่ยวกับความอันตรายของสารเคมีเพื่อความปลอดภัยในการจัดเก็บ การนำไปใช้ และการกำจัด โดยฉลากควรมีข้อมูล ดังนี้
บนฉลากบรรจุภัณฑ์มีสัญลักษณ์แสดงความเป็นอันตรายที่สื่อความหมายได้ชัดเจนเพื่อให้ผู้ใช้สังเกตได้ง่าย สัญลักษณ์แสดงความเป็นอันตรายมีหลายระบบ เช่น Globally Harmonized System of Classification and Labelling of Chemicals (GHS) ซึ่งเป็นระบบที่ใช้สากล
การทำปฎิบัติการเคมีส่วนใหญ่ต้องมีความเกี่ยวข้องกับสารเคมี อุปกรณ์และเครื่องมือต่างๆซึ่งผู้ทำปฎิบัติการต้องตระหนักถึงความปลอดภัยของตนเอง ผู้อื่น และสิ่งแวดล้อม
1.1.1 ประเภทของสารเคมี
สารเคมีมีหลายประเภท แต่ละประเภทมีสมบัติแตกต่างกัน สารเคมีจึงจำเป็นต้องมีฉลากที่มีข้อมูลเกี่ยวกับความอันตรายของสารเคมีเพื่อความปลอดภัยในการจัดเก็บ การนำไปใช้ และการกำจัด โดยฉลากควรมีข้อมูล ดังนี้
 |
| ตัวอย่างฉลาก |
 |
| ตัวอย่างสัญลักษณ์ในระบบ GHS |
ก่อนทำปฎิบัติการ
1.ศึกษาขั้นตอนหรือวิะีการทำปฎิบัตัการให้เข้าใจ วางแผนการทดลอง
2.ศึกษาข้อมุลของสารเคมีที่ใช้ในการทดลอง เทคนิคการใช่เครื่องมือ วัสดุอุปกรณ์
3.แต่งกายให้เหมาะสม
ขณะทำปฎิบัติการ
1.ข้อปฎิบัติโดยทั่วไป
1.1 สวมแว่นตานิรภัย สวมเสืิ้อคลุมปฎิบัติการที่ติดกระดุมทุกเม้ดควรสวมถุงมือ และสวมผ้าปิดปาก ควรทำในที่ที่มีอากาสถ่ายเท
1.2 ห้ามรับประทานอาหารและเครื่องดื่ม หรือกิจกรรมอื่นที่ไม่เกี่ยวข้อง
1.3 ไม่ทำการทดลองในห้องปฎิบัติการตามลำพังเพียงคนเดียว
1.4 ไม่เล่นและไม่รบกวนผู้อื่นในขณะที่ทำปฎิบัติการ
1.5 ปำิบัติตามขั้นตอนและวิธีการอย่างเคร่งครัด ไม่ทำการทดลองใดๆ ที่นอกเหนือจากที่ได้รับมอบหมาย
1.6 ไม่ปล่อยให้อุปกรณืให้ความร้อนทำงานโดยไม่มีคนดูแล
2.ข้อปฎิบัติในการใช้สารเคมี
2.1 อ่านชื่อสารเคมีบนฉลากให้แน่ใจก่อนนำไปใช้
2.2 การเคลื่อนย้าย การแบ่ง และการถ่ายเทสารเคมีต้องทำด้วยความระมัดระวัง โดยเแพาะอย่างยิ่งสารอันตราย และควรใช้อุปกรณ์
2.3 การทำปฎิกิริยาของสารในหลอดทดลอง ต้องหันปากหลอดทดลองออกจากตัวเองและผู้อื่น
2.4 ห้ามชิมหรือสุดดมสารเคมีโดยตรง ถ้าจำเป็นต้องทดสอบกลิ่นให้ใช้มือดบกให้ไอของสารเข้าจมุกเพียงเล้กน้อย
2.5 การเจือจางกรด ห้ามเทน้ำลงกรดแต่ให้เทกรดลงน้ำ
2.6 ไม่เทสารเคมีที่เหลือจากการเทหรือตักออกจากขวดสารเคมีแล้วกลับเข้าขวดอย่างเด้ดขาด ให้เทใส่ภาชนะทิ้งสารที่จัดเตรียมไว้
2.7 เมื่อสารเคมีหกในปริมาณเล้กน้อยให้กวาดหรือเช็ด แล้วทิ้งลงในภาชนะสำหรับทิ้งสารที่เตรียมไว้ หากหกในปริมารมากให้แจ้งครูผู้สอน
หลังทำปฎิบัติการ
1. ทำความสะอาดอุปกรณ์ เครื่องแก้ว และวางหรือเก็บในบริเวณที่จัดเตรียมไว้ รวมทั้งทำความสะอาดโต๊ะทำปฎิบัติการ
2. ก่อนออกจากห้องปฎิบัติการให้ถอดอุปกรณ์ป้องกันอันตราย
1.1.3 การกำจัดสารเคมี
1. สารเคมีืี่เป็นของเหลวไม่อันตรายที่ละลายน้ำได้และมี pHเป็นกลาง ปริมาณไม่เกิน 1 ลิตร สามารถเทลงอ่างน้ำและเปิดตาน้ำตามมากๆได้
2. สารละลายเข้มข้นบางชนิด เช่น กรดไอโรคลอลิก โซเดียมไอดรอกไซด์ ไม่ควรทิ้งลงอ่างน้ำหรือท่อน้ำทันที ควรเจือจางก่อนเทลงอ่างน้ำ ถ้ามีปริมารมากต้องทำให้เป็นกลางก่อน
3. สารเคมีที่เป็นของแข็งไม่อันตราย ปริมาณไม่เกิน 1 กก. สามารถใส่ในภาชนะที่ปิดมิดชิดพร้อมทั้งติดแลากชื่อให้ชัดเจน
4. สารไวไฟ ตัวทำละลายที่ไม่ละลายน้ำ สารประกอบของโลหะเป็นพิา หรือสารที่ทำปฏิกิริยากับน้ำ ห้ามทิ้งลงอ่างน้ำ ให้ทิ้งในภาชนะที่จัดเตรียมไว้
1.2 อุบัติเหตุจากสารเคมี
การปฐมพยาบาลเมื่อร่างกายสัมผัสกับสารเคมี
1.ถอดเสื้อผ้าบรเวรที่เปื้อนสารเคมีออก และวับสารเคมีออกจากร่างกายให้มากที่สุด
2. กรณีเป็นสารเคมีที่ละลายน้ำได้ ปล่อยให้น้ำไหลผ่าน
3. กรณีเป็นสารเคมีที่ไม่ละลายน้ำ ให้ล้างด้วยสบู่
4. หากทราบว่าสารเคมีที่สัมผัสร่างกายคือสารใด ให้ปฎิบัติตามใข้อกำหนด
การปฐมพยาบาลเมื่อสารเคมีเข้าตา
ตะแคงศีรษะดดยให้ตาด้านที่สัมผัสสารเคมีอยู่ด้านล่าง ล้างตาโดยการเปิดน้ำเบาๆ ไหลผ่านดั้งจมูกให้น้ำไหลผ่านตาข้างที่โดนสารเคมี
การปฐมพยาบาลเมื่อสุดดมแก๊สพิษ
1. ทำความสะอาดอุปกรณ์ เครื่องแก้ว และวางหรือเก็บในบริเวณที่จัดเตรียมไว้ รวมทั้งทำความสะอาดโต๊ะทำปฎิบัติการ
2. ก่อนออกจากห้องปฎิบัติการให้ถอดอุปกรณ์ป้องกันอันตราย
1.1.3 การกำจัดสารเคมี
1. สารเคมีืี่เป็นของเหลวไม่อันตรายที่ละลายน้ำได้และมี pHเป็นกลาง ปริมาณไม่เกิน 1 ลิตร สามารถเทลงอ่างน้ำและเปิดตาน้ำตามมากๆได้
2. สารละลายเข้มข้นบางชนิด เช่น กรดไอโรคลอลิก โซเดียมไอดรอกไซด์ ไม่ควรทิ้งลงอ่างน้ำหรือท่อน้ำทันที ควรเจือจางก่อนเทลงอ่างน้ำ ถ้ามีปริมารมากต้องทำให้เป็นกลางก่อน
3. สารเคมีที่เป็นของแข็งไม่อันตราย ปริมาณไม่เกิน 1 กก. สามารถใส่ในภาชนะที่ปิดมิดชิดพร้อมทั้งติดแลากชื่อให้ชัดเจน
4. สารไวไฟ ตัวทำละลายที่ไม่ละลายน้ำ สารประกอบของโลหะเป็นพิา หรือสารที่ทำปฏิกิริยากับน้ำ ห้ามทิ้งลงอ่างน้ำ ให้ทิ้งในภาชนะที่จัดเตรียมไว้
1.2 อุบัติเหตุจากสารเคมี
การปฐมพยาบาลเมื่อร่างกายสัมผัสกับสารเคมี
1.ถอดเสื้อผ้าบรเวรที่เปื้อนสารเคมีออก และวับสารเคมีออกจากร่างกายให้มากที่สุด
2. กรณีเป็นสารเคมีที่ละลายน้ำได้ ปล่อยให้น้ำไหลผ่าน
3. กรณีเป็นสารเคมีที่ไม่ละลายน้ำ ให้ล้างด้วยสบู่
4. หากทราบว่าสารเคมีที่สัมผัสร่างกายคือสารใด ให้ปฎิบัติตามใข้อกำหนด
การปฐมพยาบาลเมื่อสารเคมีเข้าตา
ตะแคงศีรษะดดยให้ตาด้านที่สัมผัสสารเคมีอยู่ด้านล่าง ล้างตาโดยการเปิดน้ำเบาๆ ไหลผ่านดั้งจมูกให้น้ำไหลผ่านตาข้างที่โดนสารเคมี
 |
| การปฐมพยาบาลเมื่อสารเคมีเข้าตา |
1. เมื่อมีแก๊สพิษเกิดขึ้น ต้องรีบออกจากบริเวรนั้นและไปบริเวรที่มีอากาสถ่ายเทสะดวก
2. หากผุ้ที่สุดดมแกีสพิษหมดสติหรือช่วยเหลือตัวเองไม่ได้ให้นำตัวออกจากบริเวรนั้นทันที ดดยผุ้ช่วยต้องสวมชุดป้องกัน
3. ปลดเสื้อผ้าเพื่อให้ผู้ประสบอุบัติเหตุหายใจสะดวกขึ้น
4. สังเกตการเต้นของหัวใจและการหายใจ หากว่าหัวใจหยุดเต้นและไม่หายใจให้ทำการนวดหัวใจแล้วนำส่งรพ.ทันที
การปฐมพยาบาลเมื่อโดนความร้อน
แช่น้ำเย็นหรือปิดแผลด้วยผ้าชุบน้ำจนหายปวดแสบปวดร้อน แล้วทายาขี้ผึ้งสำหรับไฟไหม้และน้ำร้อนลวก หากเกิดบาดแผลใหญ่ให้นำส่งแพทย์
1.3 การวัดปริมารสาร
ความน่าเชื่อถือของข้อมูล สามารถพิจารณาได้จาก 2 ส่วนด้วยกัน คือ ความเที่ยง (precision)และความแม่น (accuracy) ของข้อมูล โดยความเที่ยง คือ ความใกล้เคียงกันของค่าที่ได้จากการวัดซ้ำ ส่วนความแม่น คือ ความใกล้เคียงของค่าเฉลี่ยจากการวัดซ้ำเทียบกับค่าจริง
1.3.1 อุปกรณ์วัดปริมาตร
เป็นอุปกรณ์ในห้องปฏิบัติการทางวิทยาศาสตร์ ใช้สำหรับวัดปริมาตรของเหลวที่ต้องการความแม่นยำ (accuracy) สูง มีขีดและตัวเลขแสดงปริมาตร ซึ่งได้รับการสอบเทียบและกำหนดความคลาดเคลื่อนที่ยอมรับได้ (tolerance of error)
อุปกรณ์วัดปริมาตร ได้แก่
1. ปิเปตต์ (pipette)
2. บีกเกอร์ (beaker)
3. บิวเรตต์ (burette)
4. หลอดหยด (dropper)
5. หลอดฉีดยา (syringe)
6. กระบอกตวง (cylinder)
7. ขวดวัดปริมาตร (volumetric flask)
อุปกรณ์วัดปริมาตร ได้แก่
1. ปิเปตต์ (pipette)
2. บีกเกอร์ (beaker)
3. บิวเรตต์ (burette)
4. หลอดหยด (dropper)
5. หลอดฉีดยา (syringe)
6. กระบอกตวง (cylinder)
7. ขวดวัดปริมาตร (volumetric flask)
1.3.2 อุกรณ์วัดมวล
เครื่องชั่ง เป็นอุปกรณ์สำหรับวัดมวลของสารทั้งที่เป็นของแข็งและของเหลว ความน่าเชื่อถือของค่ามวลที่วัดได้ขึ้นอยุ่กับความละเอียดของเครื่องชั่งและวิะีการใช้เครื่องชั่ง เครื่องมือที่ใช้ในห้องปฎิบัติการเคมีโดยทั่วไปมี 2 แบบ เครื่องชั่งแบบสามคานและเครื่องชั่งไฟฟ้า
 |
| เครื่องชั่งไฟฟ้า |
 |
| เครื่องชั่งแบบสามคาน |
จำนวนหลักของตัวเลขที่แสดงความเที่ยงตรงของปริมาณที่วัดหรือคำนวณได้ ดังนั้นตัวเลขนัยสำคัญจึงประกอบด้วยตัวเลขทุกตัวที่แสดงความแน่นอน (certainty) รวมกับตัวเลขอีกตัวหนึ่งที่แสดงความไม่แน่นอน (uncertainty) ซึ่งขึ้นอยู่กับอุปกรณ์ที่เราเลือกใช้ด้วย
การนับเลขนัยสำคัญ
1. ตัวเลขที่ไม่มีเลขศูนย์ทั้งหมดนับเป็นเลขนัยสำคัญ
2. เลขศูนย์ที่อยู่ระหว่างตัวเลขอื่น นับเป็นเลขนัยสำคัญ
3. เลขศูนย์ที่อยู่หน้าตัวเลขอื่น ไม่นับเป็นเลขนัยสำคัญ
4. เลขศูนย์ที่ีอยู่หลังตัวเลขอื่นที่อยุ่หลังทสนิยม นับเป็นเลขนัยสำคัญ
5.เลขศูนย์ที่อยู่หลังเลขอื่นที่ไม่มีทสนิยม อาจนับหรือไม่นับเป็นเลขนัยสำคัญก้ได้
6. ตัวเลขที่แม่นตรง เป็นตัวเลขที่ทราบค่าแน่นอนมีเลขนัยสำคัญเป็นอนันต์
7. ข้อมูลที่มีค่าน้อยๆ หรือมากๆ ให้เขียนในรูปของสัญกรณ์วิทยาศาสตร์โดยตัวเลขสัมประสิทธิ์ทุกตัวนับเป็นเลขนัยสำคัญ
การปัดตัวเลข
พิจารณาจากตัวเลขที่อยู่ถัดจากตำแหน่งที่ต้องการ ดังนี้
1.กรณีตัวเลขถัดจากตำแหน่งที่ต้องการมีค่าน้อยกว่า 5 ให้ตัดตัวเลขที่อยุ่ถัดไปทั้งหมด
2. กรณีตัวเลขถัดจากตำแหน่งที่ต้องการมีค่ามากกว่า 5 ให้เพิ่มของตัวเลขตำแหน่งสุดท้ายทิ้งที่ต้องการอีก 1
3. กรรีที่ตัวเลขถัดจากตำแหน่งที่ต้องการมีค่าเท่ากับ 5 และมีตัวเลขอื่นที่ไม่ใช่ 0 ต่อจากเลข 5 ให้เพิ่มค่าของตัวเลขตำแหน่งสุดท้ายที่ต้องการอีก 1
4. กรณีที่ตัวเลขถัดจากตำแหน่งที่ต้องการมีค่าเท่ากับ 5 และไม่มีเลขอื่นต่อจากเลข 5 ต้องพิจารณาตัวเลขที่อยู่หน้าเลข 5
การบวกและการลบ
ในการบวกและลบ ผลลัพธ์ที่ได้จะมีจำนวนตัวเลขที่อยู่หลังจุดทศนิยมเท่ากับข้อมูลที่มีจำนวนตัวเลขที่อยู่หลังจุดทสนิยมน้อยที่สุด
การคูณและการหาร
ในการคูณและการหาร ผลลัพธ์ที่ได้จะมีจำนวนเลขนัยสำคัยเท่ากับข้อมูลที่มีเลขนัยสำคัญน้อยที่สุด 1.4 หน่วยวัด
1.4.1 หน่วยวัดในระบบเอสไอ
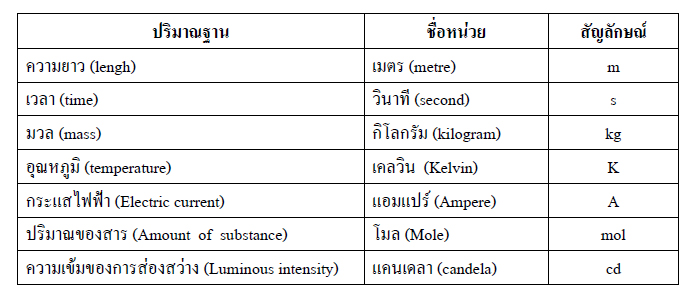
เป็นหน่วยที่ระบบหน่วยวัดระหว่างประเทศกำหนดไว้เป็นพื้นฐาน โดยหน่วย เอสไออื่นๆที่เรียกว่าหน่วยอนุพันธ์เอสไอ จะเกิดจากการนำหน่วยฐานเอสไอมาประกอบกันทั้งหมด หน่วยฐานเอสไอมีทั้งหมด 7 หน่วย
1.5 วิธีการทางวิทยาศาสตร์
พิจารณาจากตัวเลขที่อยู่ถัดจากตำแหน่งที่ต้องการ ดังนี้
1.กรณีตัวเลขถัดจากตำแหน่งที่ต้องการมีค่าน้อยกว่า 5 ให้ตัดตัวเลขที่อยุ่ถัดไปทั้งหมด
2. กรณีตัวเลขถัดจากตำแหน่งที่ต้องการมีค่ามากกว่า 5 ให้เพิ่มของตัวเลขตำแหน่งสุดท้ายทิ้งที่ต้องการอีก 1
3. กรรีที่ตัวเลขถัดจากตำแหน่งที่ต้องการมีค่าเท่ากับ 5 และมีตัวเลขอื่นที่ไม่ใช่ 0 ต่อจากเลข 5 ให้เพิ่มค่าของตัวเลขตำแหน่งสุดท้ายที่ต้องการอีก 1
4. กรณีที่ตัวเลขถัดจากตำแหน่งที่ต้องการมีค่าเท่ากับ 5 และไม่มีเลขอื่นต่อจากเลข 5 ต้องพิจารณาตัวเลขที่อยู่หน้าเลข 5
การบวกและการลบ
ในการบวกและลบ ผลลัพธ์ที่ได้จะมีจำนวนตัวเลขที่อยู่หลังจุดทศนิยมเท่ากับข้อมูลที่มีจำนวนตัวเลขที่อยู่หลังจุดทสนิยมน้อยที่สุด
การคูณและการหาร
ในการคูณและการหาร ผลลัพธ์ที่ได้จะมีจำนวนเลขนัยสำคัยเท่ากับข้อมูลที่มีเลขนัยสำคัญน้อยที่สุด 1.4 หน่วยวัด
1.4.1 หน่วยวัดในระบบเอสไอ
เป็นหน่วยที่ระบบหน่วยวัดระหว่างประเทศกำหนดไว้เป็นพื้นฐาน โดยหน่วย เอสไออื่นๆที่เรียกว่าหน่วยอนุพันธ์เอสไอ จะเกิดจากการนำหน่วยฐานเอสไอมาประกอบกันทั้งหมด หน่วยฐานเอสไอมีทั้งหมด 7 หน่วย

หน่วยนอกระบบเอสไอ นอกจากหน่วยในระบบเอสไอแล้ว ในทางเคมียังมีหน่วยอื่นที่ได้รับการยอมรับและมีการใช้กันอย่างแพร่หลาย
1.4.2 แฟกเตอรืเปลี่ยนหน่วย
เป็นอัตราส่วนระหว่างหน่วยที่แตกต่างกันสองหน่วยที่มีปริมาณเท่ากัน ตัวอย่างดังนี้
จากความสัมพันธ์พลังงาน 1 cal = 4.2 J
เมื่อใช้1 cal หารทั้งสองข้างจะได้เป็น
1 cal / 1 cal = 4.2 J / 1 cal
1 = 4.2 J / 1 cal
หรือถ้าใช้ 4.2 J หารทั้งสองข้างจะได้เป็น
1 cal / 4.2 J = 4.2 J / 4.2 J
1 cal / 4.2 J = 1
ดังนั้นแฟกเตอร์เปลี่ยนหน่วยเขียนได้เป็น 1 cal / 4.2 J หรือ 4.2 J / 1 cal
วิธีการเทียบหน่วย
ทำได้โดยการคูณปริมาณในหน่วยเริ่มต้นด้วยแฟกเตอร์เปลี่ยนหน่วยที่มีหน่วยที่ต้องการอยู่ด้านบนตามสมการ
ปริมาณและหน่วยที่ต้องการ = ปริมาณและหน่วยเริ่มต้น * หน่วยที่ต้องการ / หน่วยเริ่มต้น
1 cal / 4.2 J = 1
ดังนั้นแฟกเตอร์เปลี่ยนหน่วยเขียนได้เป็น 1 cal / 4.2 J หรือ 4.2 J / 1 cal
วิธีการเทียบหน่วย
ทำได้โดยการคูณปริมาณในหน่วยเริ่มต้นด้วยแฟกเตอร์เปลี่ยนหน่วยที่มีหน่วยที่ต้องการอยู่ด้านบนตามสมการ
ปริมาณและหน่วยที่ต้องการ = ปริมาณและหน่วยเริ่มต้น * หน่วยที่ต้องการ / หน่วยเริ่มต้น
1.5 วิธีการทางวิทยาศาสตร์
1.การสังเกตเป็นจุดเริ่มต้นของการได้ข้อมูลเกี่ยวกับสิ่งที่ต้องศึกษาโดยอาศัยประสาทสัมผัสทั้ง 5 คือการมองเห็นการฟังเสียงการได้กลิ่นการรับรสและการสัมผัส
2.การตั้งสมมติฐาน ในการคาดคะเนคําตอบของปัญหาหรือคำตอบของ คำถาม โดยมีพื้นฐานจากการสังเกตความรู้หรือประสบการณ์เดิมโดยทั่วไปสมมุติฐานจะเขียนอยู่ในรูปของข้อความที่แสดงเหตุ ผลหรืออีกนัยหนึ่งจะเป็นความสัมพันธ์ของตัวแปรต้นและตัวแปรตาม 3.การตรวจสอบสมมติฐานเป็นกระบวนการการหาคำตอบของสมมติฐานโดยมีการออกแบบทดลองให้มีการควบคุมปัจจัยต่างๆ
4.การรวบรวมข้อมูลและการวิเคราะห์ผลเป็นการนำข้อมูลที่ได้จากการ สังเกตการตรวจสอบสมมติฐานมารวบรวมวิเคราะห์และอธิบายข้อเท็จจริง
5.การสรุปผลเป็นการสรุปความรู้หรือข้อเท็จจริงที่ได้จากการตรวจสอบสมมติฐานและมีการเปรียบเทียบกับสมมติฐานที่ตั้งไว้ก่อนหน้า




ไม่มีความคิดเห็น:
แสดงความคิดเห็น